Entrez un mot ou une phrase dans n'importe quelle langue 👆
Langue:
Traduction et analyse de mots par intelligence artificielle ChatGPT
Sur cette page, vous pouvez obtenir une analyse détaillée d'un mot ou d'une phrase, réalisée à l'aide de la meilleure technologie d'intelligence artificielle à ce jour:
- comment le mot est utilisé
- fréquence d'utilisation
- il est utilisé plus souvent dans le discours oral ou écrit
- options de traduction de mots
- exemples d'utilisation (plusieurs phrases avec traduction)
- étymologie
Qu'est-ce (qui) est Перманганатометрия - définition
ПЕРМАНГАНАТОМЕТРИЯ
титриметрический метод количественного анализа, основан на окислении исследуемого вещества перманганатом калия.
Перманганатометрия
(îò Ïåðìàíãàíàòû è ...ìåòðèÿ (Ñì. ...метрия))
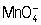
метод химического титриметрического анализа (См. Титриметрический анализ), основанный на применении растворов перманганата калия (См. Перманганат калия) (KMnO4) для количественных объёмных определений (см. Количественный анализ, Объёмный анализ). Преимущество П. заключается в том, что для неё отпадает необходимость в применении специального индикатора при установлении точки эквивалентности, так как раствор KMnO4 имеет характерный фиолетово-красный цвет. В большинстве случаев титрование восстановителей [например, Fe (ll) и Mn (II), Mo (III) и Ti (lll), 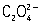 ,
, 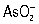 ,
, 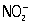 , H2O2] стандартным раствором (См. Стандартный раствор) KMnO4 проводится в кислой среде; окислительно-восстановительная реакция протекает тогда по схеме:
, H2O2] стандартным раствором (См. Стандартный раствор) KMnO4 проводится в кислой среде; окислительно-восстановительная реакция протекает тогда по схеме: 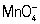 + 8H+ + 5e- ⇔ Mn2+ + 4H2O. Некоторые вещества (например, сульфиты, сульфиды, тиосульфаты, гидразин) окисляются легче в нейтральной или щелочной среде: в этом случае реакция идёт по схеме:
+ 8H+ + 5e- ⇔ Mn2+ + 4H2O. Некоторые вещества (например, сульфиты, сульфиды, тиосульфаты, гидразин) окисляются легче в нейтральной или щелочной среде: в этом случае реакция идёт по схеме:
+ 4H+ + 3е- = MnO2 + 2H2O.
Ряд металлов (Ca, Mg, Zn, La, Th) определяют, сочетая метод осаждения (в виде оксалатов) и П.
Лит. см. при ст. Оксидиметрия.
Перманганатометрия
Перманганатометрия — это титриметрический (объёмный) метод определения веществ, основанный на реакциях окисления с участием перманганат-ионов.
Wikipédia
Перманганатометрия
Перманганатометрия — это титриметрический (объёмный) метод определения веществ, основанный на реакциях окисления с участием перманганат-ионов.

